
Các nhà khoa học Đại học Pennsylvania đã phát hiện hợp chất mới từ nấm độc Aspergillus flavus, có khả năng tiêu diệt tế bào ung thư bạch cầu mạnh mẽ, cạnh tranh với thuốc điều trị hiện tại. Hợp chất này mở ra hướng đi mới trong nghiên cứu thuốc chống ung thư có nguồn gốc tự nhiên.
Các nhà nghiên cứu do Đại học Pennsylvania dẫn đầu đã biến một loại nấm độc thành một hợp chất có khả năng chống ung thư mạnh mẽ. Sau khi phân lập một nhóm phân tử mới từ Aspergillus flavus, một loại nấm gây độc cho mùa màng và đã được liên kết với cái chết trong các cuộc khai quật mộ cổ, các nhà khoa học đã biến đổi các hóa chất này và thử nghiệm trên tế bào bạch cầu. Kết quả? Một hợp chất có tiềm năng tiêu diệt ung thư, cạnh tranh với các thuốc được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) cho phép, và mở ra những hướng đi mới trong khám phá các loại thuốc từ nấm.
“Các loài nấm đã cho chúng ta penicillin,” theo lời Sherry Gao, Phó Giáo sư Hiến chương Penn trong Kỹ thuật Hóa học & Sinh học và trong Kỹ thuật Sinh học, đồng thời là tác giả cao cấp của bài báo đăng trên Nature Chemical Biology. “Những kết quả này cho thấy còn rất nhiều loại thuốc có nguồn gốc từ sản phẩm thiên nhiên vẫn chờ được phát hiện.”
Từ lời nguyền đến phương thuốc
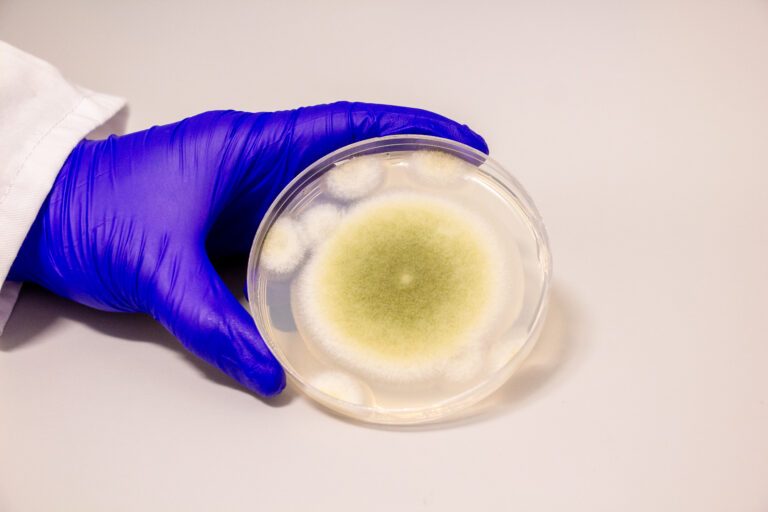
Nấm A. flavus, nổi tiếng với bào tử màu vàng, từ lâu đã được xem như một “kẻ xấu vi sinh”. Sau khi các nhà khảo cổ mở lăng mộ của vua Tutankhamun vào những năm 1920, một loạt các cái chết bất thường trong đội khai quật đã thúc đẩy những lời đồn về lời nguyền của pharaoh. Nhiều thập kỷ sau đó, các bác sĩ đã đặt giả thuyết rằng bào tử nấm, ngủ yên trong hàng thiên niên kỷ, có thể đã góp phần gây ra.
Vào những năm 1970, mười hai nhà khoa học cùng vào lăng mộ của Casimir IV tại Ba Lan. Trong vài tuần, 10 người trong số họ đã chết. Sau đó người ta phát hiện lăng mộ chứa A. flavus, mà độc tố của nó có thể gây nhiễm trùng phổi, đặc biệt với những người có hệ miễn dịch suy giảm.
Giờ đây, chính loại nấm đó lại là nguồn gốc bất ngờ của một liệu pháp ung thư đầy hứa hẹn.
Một phát hiện nấm quý hiếm
Liệu pháp được nhắc đến ở đây là một lớp peptide được tổng hợp qua ribosome và sau đó được biến đổi — gọi là RiPPs (ribosomally synthesized and post-translationally modified peptides). Tên gọi này đề cập đến cách thức hợp chất được tạo ra — bởi ribosome, cấu trúc tế bào làm protein — và việc nó được biến đổi sau đó để tăng khả năng tiêu diệt ung thư.
“Việc tinh sạch những hóa chất này rất khó,” theo lời Qiuyue Nie, nghiên cứu sau tiến sĩ trong nhóm Kỹ thuật Hóa học & Sinh học và là tác giả đầu của bài báo. Mặc dù đã có hàng ngàn RiPPs được phát hiện trong vi khuẩn, chỉ rất ít được tìm thấy trong nấm. Một phần nguyên nhân là vì các nhà nghiên cứu trước đây thường nhầm lẫn RiPPs của nấm với peptide không ribosomal và ít hiểu biết về cách mà nấm tạo ra các phân tử này. “Việc tổng hợp các hợp chất này rất phức tạp,” Nie nói thêm. “Nhưng chính điều đó cũng mang lại hoạt tính sinh học đáng chú ý cho chúng.”
Săn tìm các hợp chất
Để tìm thêm các RiPPs từ nấm, các nhà nghiên cứu đầu tiên quét khoảng một chục chủng Aspergillus, theo gợi ý của các nghiên cứu trước đó rằng các chủng này có thể chứa nhiều hợp chất loại này.
Bằng cách so sánh các hóa chất được sản sinh từ các chủng này với các khối xây dựng RiPP đã biết, nhóm nghiên cứu đã xác định A. flavus là ứng viên đầy hứa hẹn để nghiên cứu sâu hơn.
Phân tích di truyền chỉ ra một protein trong A. flavus có vai trò quan trọng như nguồn gốc các RiPPs của nấm. Khi các nhà nghiên cứu tắt các gen tạo ra protein đó, các dấu hiệu hóa học chỉ ra sự hiện diện của RiPPs cũng biến mất.
Cách tiếp cận mới này — kết hợp thông tin chuyển hóa và thông tin di truyền — không chỉ xác định được nguồn gốc của RiPPs trong A. flavus, mà còn có thể được dùng để tìm các RiPPs nấm khác trong tương lai.
Một loại thuốc mới mạnh mẽ
Sau khi tinh sạch bốn RiPPs khác nhau, các nhà khoa học phát hiện ra rằng các phân tử đều chia sẻ cấu trúc độc đáo gồm các vòng đan xen nhau. Họ đã đặt tên các phân tử này là asperigimycins, theo tên nấm nơi chúng được tìm thấy — một loại hợp chất chưa từng được mô tả trước đây.
Ngay cả khi không được biến đổi, khi trộn với tế bào ung thư của người, asperigimycins cũng thể hiện tiềm năng y học: hai trong bốn biến thể có hiệu quả mạnh mẽ với tế bào bạch cầu.
Một biến thể khác, mà các nhà nghiên cứu thêm vào một phân tử lipid (một phân tử béo) — cũng có trong sữa hoàng gia nuôi ong — cho kết quả tương đương với cytarabine và daunorubicin, hai loại thuốc đã được FDA phê duyệt và sử dụng trong nhiều thập kỷ để điều trị bạch cầu.
Giải mã cách xâm nhập tế bào
Để hiểu vì sao lipid tăng cường hiệu quả của asperigimycins, các nhà nghiên cứu đã chọn lọc bật và tắt các gen trong tế bào bạch cầu. Một gen mang tên SLC46A3 được cho là rất quan trọng để asperigimycins có thể xâm nhập tế bào bạch cầu với lượng đủ.
Gen này giúp vật chất thoát khỏi lysosome — những túi nhỏ thu gom các chất ngoại lai vào tế bào người. “Gen này hoạt động như một cánh cổng,” Nie nói. “Nó không chỉ giúp asperigimycins vào tế bào, mà có thể hỗ trợ các ‘peptide vòng’ khác làm điều tương tự.”
Việc thêm lipid vào các hợp chất mới giúp asperigimycins dễ đi vào tế bào hơn. Giống như asperigimycins, các peptide vòng khác cũng có tính dược — gần hai chục peptide vòng đã được chấp thuận lâm sàng kể từ năm 2000 để điều trị các bệnh từ ung thư đến lupus — nhưng nhiều trong số chúng cần được biến đổi để có thể nhập tế bào ở lượng đủ.
“Biết rằng lipid có thể ảnh hưởng đến cách gen này vận chuyển hóa chất vào tế bào cho chúng ta thêm một công cụ trong phát triển thuốc,” Nie nói.
Phá vỡ phân chia tế bào
Qua các thử nghiệm thêm, các nhà nghiên cứu nhận thấy rằng asperigimycins khả năng cao can thiệp vào quá trình phân chia tế bào. “Tế bào ung thư phân chia không kiểm soát,” Gao nói. “Các hợp chất này ngăn chặn sự hình thành vi ống — rất cần thiết cho việc phân chia tế bào.”
Đáng chú ý là các hợp chất gần như không có ảnh hưởng lên tế bào ung thư vú, gan hoặc phổi — cũng như trên nhiều loại vi khuẩn và nấm — điều này cho thấy hiệu ứng của asperigimycins khá chọn lọc với một số loại tế bào nhất định, một đặc điểm quan trọng nếu chúng ta muốn phát triển thành thuốc trong tương lai.
Hướng phát triển trong tương lai
Bên cạnh việc chứng minh tiềm năng y học của asperigimycins, các nhà nghiên cứu còn xác định được các cụm gen tương tự trong các loại nấm khác, gợi ý rằng còn nhiều RiPPs từ nấm đang chờ được khám phá. “Mặc dù chỉ có vài cái được phát hiện, hầu hết đều có hoạt tính sinh học mạnh,” Nie nói. “Đây là một vùng chưa được khai thác với tiềm năng to lớn.”
Bước tiếp theo là thử asperigimycins trên mô hình động vật, với hy vọng một ngày nào đó sẽ tiến tới thử nghiệm lâm sàng trên người. “Thiên nhiên đã ban tặng cho chúng ta một dược phòng tuyệt vời,” Gao nói. “Chúng ta có nhiệm vụ khám phá bí mật của nó. Với vai trò là kỹ sư, chúng tôi rất hào hứng tiếp tục nghiên cứu, học hỏi từ thiên nhiên và sử dụng kiến thức đó để thiết kế những giải pháp tốt hơn.”
Nghiên cứu này được thực hiện tại Trường Kỹ thuật và Khoa học Ứng dụng của Đại học Pennsylvania; Đại học Rice; Đại học Pittsburgh; Trung tâm Ung thư MD Anderson của Đại học Texas; Trường Y Washington University ở St. Louis; Baylor College of Medicine và Đại học Porto.
[Đề tài nghiên cứu được hỗ trợ bởi Viện Y tế Quốc gia Hoa Kỳ (NIH) … (danh sách các mã tài trợ và đơn vị tham gia trong bài viết gốc tiếng Anh) …]
*Nguồn: Dịch tiếng Việt từ bài viết “Penn Engineers Turn Toxic Fungus into Anti-Cancer Compound” – Tác giả: Ian Scheffler (School of Engineering and Applied Science University of Pennsylvania)
Linh Chi Khang Nam

